学習内容解説ブログサービスリニューアル・受験情報サイト開設のお知らせ 学習内容解説ブログをご利用下さりありがとうございます。 開設以来、多くの皆様にご利用いただいております本ブログは、 より皆様のお役に立てるよう、2020年10月30日より形を変えてリニューアルします。 以下、弊社本部サイト『受験対策情報』にて記事を掲載していくこととなりました。 『受験対策情報』https://www.sakusakura.jp/examination/ 『受験対策情報』では、中学受験/高校受験/大学受験に役立つ情報、 その他、勉強に役立つ豆知識を掲載してまいります。 ぜひご閲覧くださいませ。今後とも宜しくお願い申し上げます。 |
こんにちは、サクラサクセスです。
このブログでは、サクラサクセスの本物の先生が授業を行います!
登場する先生に勉強の相談をすることも出来ます!
"ブログだけでは物足りない"と感じたあなた!!
ぜひ無料体験・相談をして実際に先生に教えてもらいませんか?
さて、そろそろさくらっこ君と先生の授業が始まるようです♪
今日も元気にスタート~!
白枝先生
みなさん、GWはどう過ごしましたか?
部活で忙しかったですか?どこか遠出しましたか?
10連休も長いようであっという間でしたね。
さあ、いよいよ中間テストがやってきますよ‼
高校生のみなさんは中間テスト真っ最中という人もいますよね?
今日は化学の「イオン」のお話です。
みなさん、イオンって何かわかりますか?

少し前にはマイナスイオンは癒しの効果がある※とか
話題になっていたよね!
イオンって言葉は聞いた時に耳に残りやすいんだけど、
なんだか難しくてなかなか覚えられないんだよね…
※科学的根拠はありません。
白枝先生
うんうん!
マイナスイオンはよく聞くよね!
さくらっこくんの言う通り難しく感じてしまう方が多い内容なんだけど、
仕組みを覚えれば案外簡単だな!って思えるから一緒に頑張ろう!
前回化学の話をした際に原子には腕があるという話をしましたね。
⇩読んでいない方はコチラをクリック⇩
原子は原子同士で腕を取り合ってつながっていないと、
安定して存在できないのです。
そこで異なる原子や同じ原子同士で腕を取り合ってつながっているのです。
しかし、中には腕が存在しない原子もあるのです。
それらを希ガス原子といいます。
腕が無い希ガス原子は、
他の原子とつながっていなくても安定して存在できるのです。

その希ガス原子とイオンには、どんなつながりがあるのかな??
白枝先生
他の原子が、
希ガス原子と同じ形になったものがイオンです。
イオンは水溶液の中に存在しています。
物質が液体に溶けるとき、
液の中では物質はイオンとなって存在するのです。
では、ここからイオンがどうやってできるのかを説明しましょう。
イオンが出来る仕組み
①原子の腕の正体は…
白枝先生
原子は中心に存在する核とその周りを取り囲んでいる電子によって出来ています。
例としてナトリウムを書くとちょうど下のような形です。
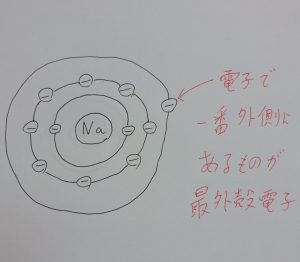
白枝先生
一番外側(最外殻)に電子が一つだけありますね。
これを最外殻電子といいます。
実は、原子の腕の正体はこの最外殻電子なのです。
電子はマイナスの電気を帯びていますから、
この電子が無くなるとマイナスが無くなって数学のようにプラスになるのです。
このように電子を失ってできるイオンを陽イオンといいます。
白枝先生
もう一つ例を挙げましょう。
今度は酸素原子です。
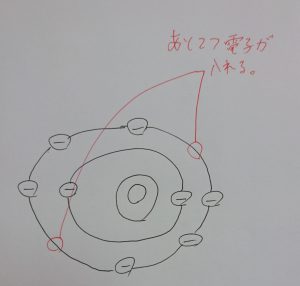
白枝先生
最外殻は電子が入れる個数が決まっています。
酸素の場合、最外殻には8個の電子が入れるのであと2個入るスペースがあります。
このスペースも原子の腕の正体です。
このスペースに電子だけが入ると最外殻が埋まります。
電子はマイナスの電気を帯びていますからマイナスをもらうことになります。
このように他から電子をもらってできるイオンを陰イオンといいます。

希ガス原子のように安定したものをイオンというんだね!
また、最外殻電子があったり、スペースが空いていたりするところが、
原子の腕の正体だったんだ!!
②イオンの書き方
白枝先生
①でナトリウムと酸素がそれぞれイオンになる過程を話しました。
それぞれイオンになった図は次のようになります。
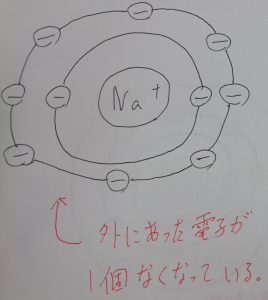
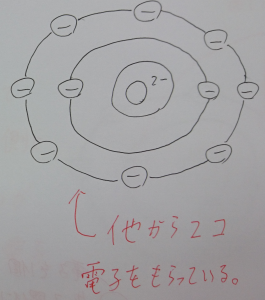
補足説明
左側のナトリウムは点線部分がなくなっていて、
右側の酸素は丸で囲まれているように2個の電子をもらっているよ!
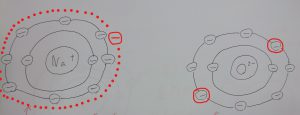
※上図の書き方は一例です。酸素がもらった電子の位置も一例です。
白枝先生
ナトリウムは電子が1個無くなっていますね。
一方酸素は電子を2個もらっています。
この2つに限らず、他の原子も同じようにしてイオンになるのです。
また、イオンも化学式のように記号で書くことができます。

白枝先生
図のような書き方をしたものをイオン式といいます。
イオン式の右上の数字は失った電子またはもらった電子の数を表します。
1個の場合は1を省略して書きます。
(※ナトリウムのように)
今回はイオンの基本的な仕組みについて説明しました。
これ以外のイオンの出来る仕組みもありますが、
まずはこの基本的な仕組みを覚えて下さい。
中学生のみなさんも3年生でイオンは習うので是非参考にしてください‼

他のイオンはどうなってるのか、とても興味がでてきた!
ナトリウムと酸素以外にも、自分で調べてみるよ!
白枝先生ありがとうございました!!
最後までお読みくださりありがとうございます♪
実際に、このブログに登場した先生に勉強の相談をすることも出来ます!
「ブログだけでは物足りない」、「もっと先生に色々教えてほしい!」と感じたあなた、
ぜひ無料体験・相談をして実際に先生に教えてもらいましょう!
友だちも誘って、ぜひ一度体験しに来てくださいね!

